Prof. Joseph Merola (Boston, Verenigde Staten) heeft een analyse gepresenteerd van de resultaten van BE SURE en BE RADIANT, twee fase III-studies die de werkzaamheid onderzochten van de IL-17A/IL-17F-remmer bimekizumab bij patiënten met matige tot ernstige plaque psoriasis.
De analyse die door J. Merola gepresenteerd werd, had als doel de invloed van twee verschillende dosisschema’s na te gaan op de plaques op de hoofdhuid, de nagels en de handpalmen en voetzolen.
Er werd een analyse gemaakt van de samengevoegde gegevens van de patiënten met matige tot ernstige psoriasis vulgaris die deelnamen aan de studies BE RADIANT en BE SURE en die eerst gerandomiseerd werden naar bimekizumab 320mg om de 4 weken (Q4W) tot week 16, en vervolgens verder bimekizumab Q4W (Q4W/Q4W) kregen of overgeschakeld werden op bimekizumab 320mg om de 8 weken (Q4W/Q8W) tijdens de onderhoudsperiode.
Om in de studies opgenomen te worden, moesten de patiënten bij aanvang van de studie psoriasis op een bepaalde lichaamszone vertonen: score voor de hoofdhuid van ≥ 3 (5-puntenschaal [0-4]) op de Investigator’s Global Assessment (IGA), score voor de nagels van > 10 op de modified Nail Psoriasis Severity Index (mNAPSI) (totale score voor de nagels op een schaal van 0-130) of een score voor de handpalmen en de voetzolen van ≥ 3 op de (pp)-IGA (5-puntenschaal [0-4]). Het doel van de studie was om na te gaan bij welk percentage van de patiënten de letsels op één van de drie zones volledig opgeklaard waren in week 48.
De ontbrekende gegevens werden geïmputeerd naar de groep van non-responders (NRI). De kenmerken van beide groepen patiënten waren vergelijkbaar. In totaal werden er 669 patiënten opgenomen in de studies: 300 in de Q4W/Q4W-groep en 369 in de Q4W/Q8W-groep. In beide groepen vertoonden bij inclusie respectievelijk 79% en 70,7% een IGA ≥ 3, 18,7% en 13,6% een pp-IGA ≥ 3 en 31,3% en 32,8% een mNAPSI > 10.
Van de patiënten die bij aanvang een IGA ≥ 3 hadden voor de hoofdhuid vertoonde respectievelijk 80,2% en 82,0% van degenen die behandeld werden met bimekizumab Q4W/Q4W en Q4W/Q8W na 16 weken een volledige opklaring van de letsels op de hoofdhuid. In beide groepen hield die score aan tot week 48 (zie figuur) (Merola J.).
Figuur: Opklaring van de hoofdhuid in week 48 bij patiënten die aanvankelijk een IGA-score ≥ 3 hadden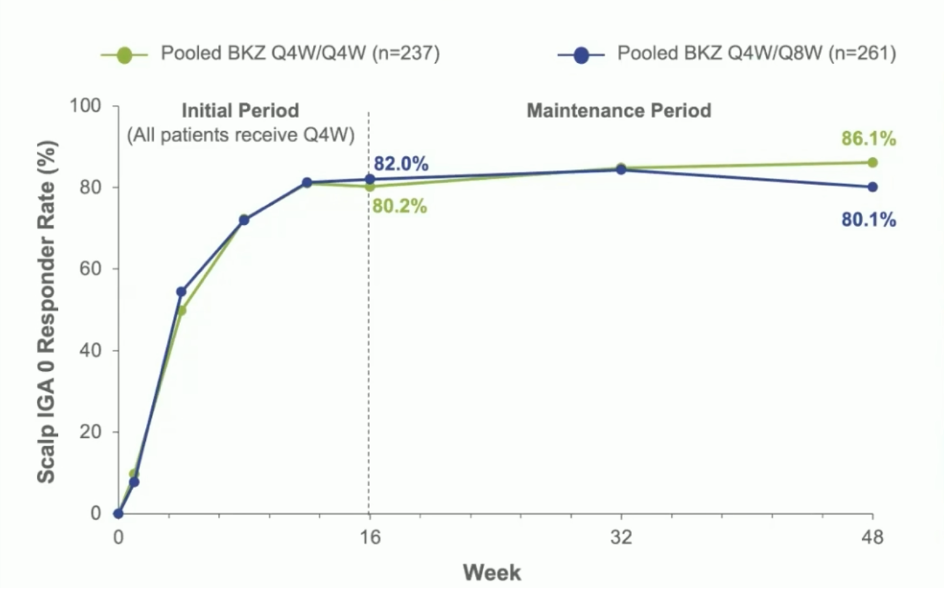
Bron figuur: Merola J. Bimekizumab efficacy in high-impact areas for patients with moderate to severe plaque psoriasis: Pooled results through 48 weeks from the BE SURE and BE RADIANT phase 3 trials EADV 2021 nr ID FC03.05)
Voor de nagels steeg het percentage patiënten met een mNAPSI-score = 0 tot week 48 en bereikte 59,6% in de Q4W/Q4W-groep en 65,3% in de Q4W/Q8W-groep.
Joseph Merola concludeerde dat de psoriasisletsels op de hoofdhuid en de handpalmen en voetzolen bij een groot deel van de behandelde patiënten in week 16 volledig verdwenen waren, en dat die respons aanhoudt tot in week 48. Bij nagelaantasting duurt het langer voor er genezing optreedt, maar dat komt vooral omdat nagels tijd nodig hebben om zich te herstellen en opnieuw te groeien. Tot slot zijn de resultaten voor opklaring vergelijkbaar ongeacht de dosis die na week 16 toegediend wordt.
Referenties:
- Merola J. Bimekizumab efficacy in high-impact areas for patients with moderate to severe plaque psoriasis: Pooled results through 48 weeks from the BE SURE and BE RADIANT phase 3 trials EADV 2021 nr ID FC03.05
- Gordon K, Foley P, Krueger J et al. Bimekizumab efficacy and safety in moderate to severe plaque psoriasis (BE READY): a multicentre, double-blind, placebo-controlled, randomised withdrawal phase 3 trial Lancet 2021; 397:475-486
- Warren RB, Blauvelt A, Bagel J et al. Bimekizumab versus Adalimumab in Plaque Psoriasis N Engl J Med 2021; 385:130-141 DOI: 10.1056/NEJMoa2102388